Faglig forklaringer til luker i julekalenderen
19. Desember – Julekule
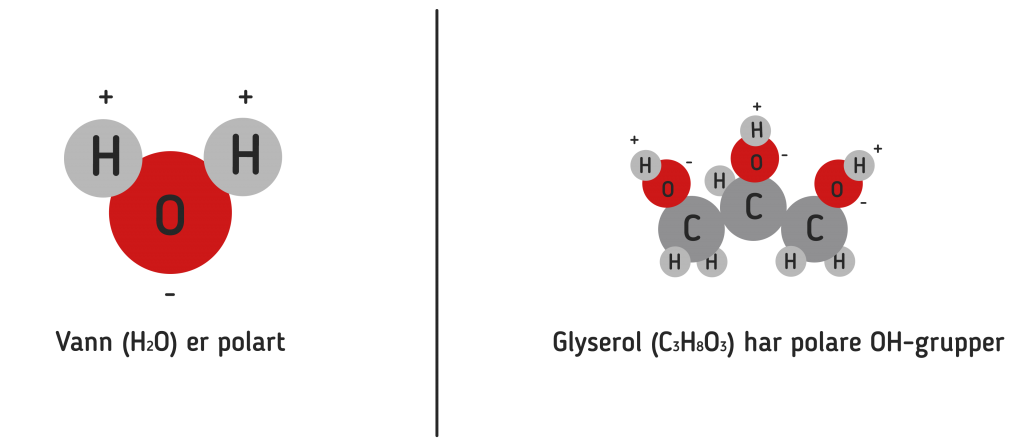
Alle stoffer i universet er bygget opp av noen stoffer som kalles grunnstoff. Et atom er den minste mengden man kan ha av et grunnstoff. Atomer kan binde seg sammen med andre atomer (både med samme type og andre grunnstoffer) og danne større partikler som kalles for molekyler. Måten et molekyl er bundet sammen kan føre til at den elektriske ladningen blir forskjøvet, og molekylet får to poler med ulik ladning (+ og -). Et eksempel på et slikt polart stoff er et vannmolekyl (H2O). Polare og upolare stoffer blander seg ikke sammen, f.eks. olje og vann. Noen molekyler kan derimot blande seg med både polare og upolare stoffer, fordi molekylet har både en polar og en upolar del.
Glyserol (C3H8O3) er en tykk, søt væske, som inngår i flere fett- og planteoljer. På grunn av glyserolmolekylets polare OH-grupper (hydroksylgrupper) kan det binde seg til vann. Noe som er viktig når vi skal lage en fin julekule!